Accueil du site > Evènements > Comptes rendus > VIIIème journée Toulousaine de Pneumo-allergologie Pédiatrique

VIIIème journée Toulousaine de Pneumo-allergologie Pédiatrique
mardi 4 janvier 2005, par
Les réunions régionales sont souvent très riches. Voici le compte-rendu des journées toulousaines de pneumo-allergologie pédiatrique qui ont eu lieu fin 2004.
Stratégie des investigations dans l’asthme du nourrisson
Pr Christophe Marguet, Rouen
Le terme « wheezing » anglo-saxon est facteur de confusion. Il traduit une réduction du calibre des voies aériennes.
– L’interrogatoire des parents est peu fiable (la valeur prédictive positive du wheezing est seulement de 53 %, 90 % pour les ronchi).
Souvent les parents parlent plutôt de toux.
L’asthme du nourrisson est le diagnostic le plus fréquent devant des sibilants, mais il faut savoir éliminer les diagnostics différentiels devant :
- l’absence d’antécédents particuliers : cardiopathie, prématurité, maladie génétique
- l’absence de signes inhabituels : croissance staturo-pondérale normale, sibilants bilatéraux, eupnéique en dehors des crises, thorax normal, absence de diarrhée.
– Le seul examen complémentaire est la radiographie thoracique dans l’asthme non compliqué. Elle est indispensable.
– La prévalence de l’asthme du nourrisson a augmenté, passant de 12 à 25 % de 1990 à 1998, de même que la prévalence de l’eczéma. Par contre la fréquence de l’eczéma parmi les siffleurs n’a pas augmenté. Ce qui confirme que ce sont 2 pathologies différentes aux relations étroites.
L’asthme du nourrisson est différent de l’asthme chronique comme en témoigne l’infiltration par des polynucléaires neutrophiles alors qu’on retrouvera des éosinophiles dans l’asthme chronique d’où un traitement différent. L’asthme du nourrisson est avant tout une bronchite chronique infectieuse (VRS et rhinovirus avant 2 ans, rhinovirus surtout après 2 ans).
– L’obstruction des voies aériennes peut être
- Dynamique primitive (dyskinésies des voies aériennes : laryngomalacie, trachéomalacie ...),
- Secondaire (compression extrinsèque).
- Elle peut être liée à une compression extrinsèque, intra-luminale (corps étranger...) ou liée à une pathologie associée.
On va rechercher une mucoviscidose, une malformation, un corps étranger, des séquelles de viroses (diagnostic différentiel ou même entité ? ).
La mucoviscidose bénéficie du dépistage depuis 2002. C’est un mode de révélation non évocateur ; ce sont des mucoviscidoses qui font une bronchiolite.
L’inhalation de corps étranger va intéresser préférentiellement des enfants de 9 à 36 mois. Le syndrome de pénétration sera absent dans un cas sur deux. Des sifflements unilatéraux avec un bruit de clapet sont hautement évocateurs. La radiographie de face en inspiration et expiration a une sensibilité de 80 %. On réalisera une fibroscopie souple en cas de doute, rigide si le diagnostic est certain.
La laryngomalacie s’accompagne d’un stridor avec plus ou moins une dyspnée inspiratoire. La biopsie si elle était réalisée montrerait une infiltration avec souvent des éosinophiles. Le diagnostic est facile, mais 17% sont associées à une trachéomalacie. On peut alors avoir un stridor qui s’aggrave après un épisode de bronchiolite qui amènera alors à la fibroscopie.
Les trachéomalacie est une bronchomalacie primitive se traduisant par une dyspnée sifflante aux deux temps avec voie rauque et un intervalle libre de 3 mois pour la trachéomalacie, variable pour la bronchomalacie. Elles sont aggravées par les infections virales.
– Le reflux gastro-oesophagien (RGO) est une association fréquente avec l’asthme du nourrisson (65%).
On recherchera notamment une douleur épigastrique avec un enfant qui s’arrête vite de manger car « il n’a plus faim ».
Les anglo-saxons parlent de micro-inhalations avec augmentation des macrophages à inclusion lipidique. Mais les macrophages lipidiques sont augmentés chez l’enfant par rapport à l’adulte.
Le traitement anti-reflux est efficace sur la douleur mais pas sur les symptômes respiratoires.
– La place des investigations reste donc limitée chez le nourrisson asthmatique.
Dans une étude sur 144 nourrissons, un bilan exhaustif a montré 2 diagnostics différentiels dont une mucoviscidose.
Dans l’étude de Marguet sur 181 nourrissons, il n’y a eu aucun diagnostic différentiel. On retrouvait un tabagisme passif dans 50 % des cas, des tests cutanés positifs aux pneumallergènes dans 28 %, aux trophallergènes dans 17%. La radiographie thoracique était anormale dans 33%.
La fibroscopie bronchique est un examen ciblé qu’on va réserver aux sifflements persistants ou en cas d’échec thérapeutique.
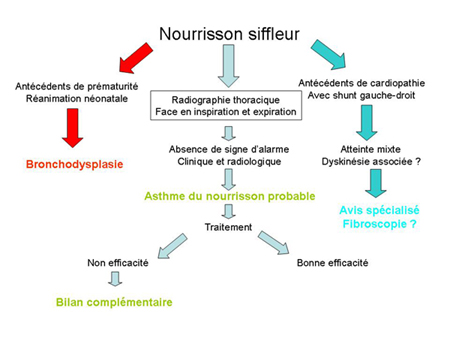
On peut donc se fier à cet algorythme :
On devra faire un bilan complémentaire en cas :
- de forme sévère inhabituelle
- de stridor, dyspnée aux deux temps, polypnée, de signes inter critiques, de déformation thoracique, de toux productive matinale, de bronchorrhée
- de signes extra-respiratoires associés : cassure pondérale, diarrhée chronique, cardiopathie, douleurs abdominales
- de terrain particulier : trisomie 21, atrésie de l’œsophage
- de radiographie thoracique anormale ou de situs inversus
Sans orientation diagnostique le bilan sera large sinon il sera ciblé en fonction de l’orientation.
– Réponses aux questions :
- En cas de syndrome lobaire moyen, l’endoscopie est systématique à la recherche d’une cardiopathie, d’une dyskinésie ou d’une compression extrinsèque.
- Le tracé de pH-métrie est différent dans les cas d’asthme, le reflux se voit alors plutôt le jour et pas la nuit contrairement au RGO en pathologie digestive.
- Les tests allergologiques sont à cibler en cas de nourrissons à risque ou en fonction de l’histoire clinique. Le Phadiatop a une très faible sensibilité chez les moins de 4 ans. Les prick-tests doivent donc être fait en première intention.
- Le dosage des immunoglobulines en cas d’échec du traitement est régulièrement bas. Attention à bien les interpréter en fonction de l’âge. Dans les formes sévères, on dose les sous-classes d’immunoglobulines. On retrouve fréquemment des taux bas d’IgG2 et d’IgG1 qui vont souvent se normaliser 6 mois plus tard.
- En cas d’échec du traitement, il faut bien sûr vérifier la technique d’inhalation. Sinon il faut faire un bilan avec facilement une fibroscopie.
Quand et comment traiter un asthme du nourrisson ?
Dr François Brémont, Toulouse
L’asthme du nourrisson est défini comme 3 épisodes de dyspnée aiguë (frein expiratoire, tirage).
Son évaluation est difficile.
Les médicaments sont difficiles à administrer.
La physiopathologie est hétérogène. 37 à 40 % des siffleurs siffleront par la suite.
On peut définir 3 groupes :
- les siffleurs transitoires qui n’auront pas d’hyperactivité bronchique (HRB),
- les siffleurs non atopiques qui vont siffler principalement lors des infections virales, ce groupe peut avoir une HRB à 10 ans
- les siffleurs atopiques.
– Qui traiter ?
Les symptomatiques sévères et/ou fréquents.
– Comment ?
Par les Glucocorticoïdes inhalés presque exclusivement.
Les études réalisées avec le BUDESONIDE et la FLUTICASONE montrent une efficacité sur le wheezing principalement quand celui-ci est fréquent ou persistant. Les études avec du BUDESONIDE nébulisé à 1 mg *2/jour ont montré la même efficacité.
Il faut au minimum 2 mois de traitement (avec la Fluticasone) pour avoir une efficacité. On a un effet dose. Par contre il n’a aucun effet sur les épisodes peu fréquents.
Dans une étude sur des enfants de 12 à 47 mois traités par Fluticasone 100 ug, 2 fois par jour versus placebo pour des symptômes fréquents (symptômes 3 jours ou plus par semaine ou plus de 75 % du temps pendant 4 semaines), on note un pourcentage de jours sans symptômes passant à 40 % avec la Fluticasone contre 20 % avec le placebo.
La différence était non significative quand les symptômes étaient peu fréquents. Par contre quand on a des antécédents familiaux d’asthme au premier degré, la différence est significative. Si on a des antécédents familiaux d’asthme et des symptômes fréquents l’amélioration est encore plus nette.
Les glucocorticoïdes au décours d’une bronchiolite grave n’ont pas montré d’effets s’il n’y avait pas d’antécédents précédant cet épisode.
Tolérance des glucocorticoïdes :
Il y a un effet dose sur la croissance. La différence entre Budéosnide 200 ug * 2 et Fluticasone 200 ug , 2 fois par jour était non significative mais différente du placebo.
Il y a un retentissement sur l’axe corticotrope d’où une nécessité de faire une surveillance du cortisol urinaire sur la créatinine sous Fluticasone à doses élevées.
Il faut donc respecter les posologies.
Les anti-leucotriènes ont montré un effet modéré sur l’asthme persistant des enfants de 2 à 5 ans avec un petit effet sur le nombre de jours avec symptômes.
Les bêta2 à longue durée d’action ne bénéficie que d’études physiologiques montrant effectivement un effet positif. Mais il n’y a aucune étude clinique et pas d’AMM.
– Quand ?
- Quand les symptômes sont sévères ou fréquents : ≥ 3 jours par semaine ou 75 % du temps pendant 4 semaines ou 2 exacerbations sévères à moins de 6 semaines d’intervalle.
- Si les symptômes sont moins fréquents (> 3 wheezing/an de durée > 1 jour et affectant le sommeil) avec un risque élevé d’asthme allergique (antécédents parentaux d’asthme, dermatite atopique, IgE totaux augmentés à 9 mois ou prick-tests positifs)
– Comment ?
La durée doit être de 3 mois. Au-delà on fait un test d’arrêt systématiquement.
La posologie doit être de 0,5 à 1 mg, 2 fois par jour pour le Budésonide en Nébulisation, 200 à 250 µg 2 fois par jour pour le Budésonide et la béclométasone en spray + chambre d’inhalation, 50 à 100 µg 2 fois par jour pour la Fluticasone.
Lors des épisodes aigus, on utilisera les bêta²-agonistes à courte durée d’action, 3 bouffées dans la chambre. Les anticholinergiques n’ont pas de place chez les moins de 2 ans. Les glucocorticoïdes per os marchent mais pas besoin d’augmenter les doses.
En cas d’échec de la chambre d’inhalation, il faut passer à la nébulisation.
Chambre d’inhalation ou nébulisation chez le nourrisson et le jeune enfant
Pr Jean-Christophe Dubus, Marseille
Le but du traitement d’urgence de la crise d’asthme est d’ouvrir les bronches le plus rapidement possible.
De 6 à 8 ans, le 1er traitement est la chambre d’inhalation. En cas d’échec, on passe à la nébulisation.
Les bêta² mimétiques ont un effet puissant, une rapidité d’action, un excellent ratio effets attendus/effets secondaires. L’administration est rapide à fortes doses que ce soit par voie inhalée ou par voie injectable.
La comparaison est difficile en fonction du produit utilisé, des doses utilisées, de la chambre d’inhalation employée en particulier en métal, de petit ou grand volume ...
Les doses sont selon l’AMM de 100 à 200 µg/prise (< 1500 µg/jour jusqu’à il y a peu de temps, plus de limite actuellement ) pour le salbutamol en aérosol doseur et en poudre, 0, 05 à 0,15 mg/kg/20 à 30 minutes en nébulisation.
Les doses des guides :
| GINA 2002 | Consensus réanimation | |
| Salbutamol Nébulisation | 0,15 mg/kg * 3 Puis 0,15 mg/kg/ 3 heures Ou 0,5 mg/kg/heure en continu | 0,05 à 0,15 mg/kg/dose (minimum 0,5 à 1,5 mg) ou doses fixes salbu/terbu |
| Salbutamol + chambre | 4 à 8 bouffées/20 min * 3 puis / 1 à 4 heures (1 bouffée = 100 µg) | > 1 an : 5 à 10 bouffées |
Les études confirment qu’il vaut mieux des fortes doses.
Une étude 0,05 mg/kg versus 0,15 mg/ kg/ prise en nébulisation montre la nette supériorité de la forte dose.
Dans une étude 0,15 mg/kg/prise versus 6-10 bouffées (0,6-1 mg) versus 2 bouffées, il n’y avait pas de différence significative entre les 3 groupes mais sur un effectif faible. L’efficacité semble moins bonne avec 2 bouffées et la fréquence cardiaque était plus augmentée avec les nébulisations.
En fonction des chambres employées on retrouve en tête la Nespacer et le Babyhaler. Il n’y a pas de données sur l’intérêt d’un petit ou d’un grand volume.
Pour l’électrostatisme, il est surtout important quand on délivre de petites quantités, en crise cela est peut-être un peu moins vrai. Le métal et le plastique sont presque identiques.
Pour la déposition pulmonaire, les chambres d’inhalation sont superposables à la nébulisation quel que soit l’âge (0,12 à 2,26 % versus 1,3 à 2,6 % chez les moins de 2 ans, 4,5 % +/- 1,4 versus 5,4 +/- 2,1 chez les 2 à 4 ans, 11,1+/- 1,7 % chez les 5-8 ans, 6 % avec l’embout sans le masque, 12 à 20 % chez l’adulte, < 1 % si fait à distance avec la chambre d’inhalation).
La Cochrane database 2003 a repris 22 études soit 1076 enfants et 444 adultes. Chez l’adulte, il n’y avait aucune différence entre chambre d’inhalation et nébulisation. Chez l’enfant, on note une petite supériorité de la chambre d’inhalation en raison d’une diminution du temps passé aux urgences et d’une diminution de la fréquence cardiaque. Il y a moins d’hypoxémie avec la chambre d’inhalation (diminution de la PaO2 sur les gaz du sang). Il n’y avait aucune étude sur la chambre d’inhalation dans des crises d’asthmes graves.
Dans une méta-analyse de 2004 chez des moins de 5 ans, la chambre d’inhalation est supérieure à la nébulisation pour les crises modérées ou graves avec un score clinique amélioré.
Les recommandations du GINA 2002 sont l’administration de préférence par la chambre d’inhalation (grade A) en sachant qu’en crise la nébulisation peut être plus facile chez l’enfant.
La chambre d’inhalation doit être utilisée avec un masque facial chez les moins de 3 ans.
L’intérêt de la chambre d’inhalation est la diminution du temps de séjour aux urgences, la diminution des hospitalisations, et le début d’apprentissage aux familles des techniques d’inhalation. Il n’y a pas de vecteur gazeux (6 à 10 litres d’O2 pour la nébulisation) et donc moins d’hypoxémie, une réduction des effets latéraux en particulier la tachycardie.
L’acceptabilité pendant la crise est bonne (hors des crises beaucoup refusent). La prise est optimale quand le masque est collé au visage, en dehors des pleurs et en aspiration buccale exclusive. Une mauvaise application du masque diminue la dose délivrée et le dépôt pulmonaire.
Mais pour la nébulisation, on retrouve les mêmes problèmes lorsque le masque est loin du visage, le mieux étant l’administration par l’intermédiaire d’un Hood de grand volume qui donne une bonne déposition et autant de dépôts sur le visage qu’avec le masque.
La chambre d’inhalation doit être lavée une fois par mois (technique Palmolive) à domicile et amenée à l’hôpital lors des crises.
À domicile, on prend la chambre du médecin. Tout dispositif artificiel comme une bouteille plastique de 500 ml ou une feuille de papier roulée sur elle-même peut être utilisé en absence de chambre.
À l’hôpital le CLIN interdit toute utilisation d’une même chambre chez différents patients sinon il faut procéder à une désinfection rigoureuse entre les 2 utilisations.
– En conclusion, à l’aube des bêta2 agonistes disponibles en nébulisation en officine, lors d’une crise d’asthme en ville la chambre d’inhalation doit être utilisée en première intention à la dose de 50 µg/kg (soit 1 bouffée par 2 kg) avec un maximum de 1 mg (10 bouffées). En cas de nébulisation celle-ci doit être faite sous O2.
À l’hôpital, la chambre d’inhalation doit être utilisée en 1ère intention, en cas de difficultés, la voie injectable ou la nébulisation peuvent être utilisées (intérêt du Hood de grand volume).
Les écoles de l’asthme
Dr Agnès Juchet, Toulouse
On peut retrouver les recommandations de Juin 2002 sur le site de l’ANAES (www.anaes.fr).
Pour l’ANAES, il faut éduquer tous les asthmatiques. Devant l’impossibilité d’une telle entreprise, on se limite aux asthmes à risque, aux niveaux socio-économiques défavorisés, aux adolescents peu compliants.
Avant on fait un diagnostic éducatif (Si tu devais expliquer ton asthme à un copain qu’est ce que tu dirais ?).
On définit les objectifs :
- bonne technique d’inhalation,
- reconnaître la crise,
- prendre régulièrement son traitement de fond, en plus du traitement spécifique adapté à chaque enfant en fonction des allergies, du diagnostic éducatif ...
Sur Toulouse, les enfants ont deux séances d’1/2 journée à 1 mois d’intervalle, pour les adolescents 1/2 journée pendant les périodes scolaires. Les parents et les enfants sont vus ensemble et séparément, en individuel et en collectif.
Les résultats sont bons d’autant plus que l’asthme est sévère et que les enfants utilisent un peak flow.
Quelle est la place du bilan allergologique dans la dermatite atopique : recommandations du consensus d’Octobre 2004.
Dr Fabienne Rancé, Toulouse
Cet exposé ayant déjà été traité sur le site dans le résumé de la conférence consensus sur la dermatite atopique je ne reprendrai que les points essentiels.
Chez l’enfant la prévalence de la dermatite atopique est de 15 à 20 % et l’on retrouve une sensibilisation IgE dans 33 à 40%.
Chez l’adulte, la prévalence est de 1 à 3 % avec 0 % de sensibilisation IgE. Il faut donc savoir rechercher une sensibilisation IgE chez l’enfant contrairement à l’adulte.
– Les tests allergologiques : quand et pour qui ?
Il faut pratiquer un bilan allergologique :
- En cas d’eczéma atopique (EA) et de signes évocateurs d’une allergie : urticaire aiguë, syndrome oral, asthme...
- En cas de traitement corticoïde correct avec une mauvaise efficacité ce celui-ci.
Dans ce cas, on retrouve beaucoup plus fréquemment des allergies alimentaires associées.
D’autant qu’on retrouve des facteurs associés :- Antécédents familiaux d’atopie : Le risque d’asthme est plus important en cas d’EA et d’histoire familiale d’atopie.
- Allergie alimentaire associée : La sensibilisation ou l’allergie alimentaire à l’œuf expose au risque d’asthme (Odd ratio de 4,4).
- EA sévère
- EA de début précoce.
Parmi les facteurs les plus déterminants pour le risque d’asthme ultérieur on retrouve des tests cutanés positifs à 4 ans, une allergie alimentaire, une rhinite à 4 ans, un asthme maternel et un tabagisme passif.
Le bilan allergologique est un marqueur de l’évolution. Dans l’étude de Novembre, aucun des enfants souffrant d’EA non sensibilisés n’ont développé d’asthme lors du suivi jusqu’à l’âge de 11 ans.
– Les tests allergologiques : lesquels ?
Le bilan allergologique doit comprendre l’histoire clinique, l’examen clinique, les tests cutanés, les tests épicutanés, les IgE spécifiques et si besoin les tests de provocation orale.
Les principaux allergènes à tester en prick-test avant l’âge de 3 -4 ans sont essentiellement les aliments : le lait de vache, l’œuf, l’arachide, la noisette, le poisson, la moutarde ainsi que les acariens voir plus – Définition et les phanères de chat.
Après 3-4 ans, on doit rajouter aux allergènes alimentaires (œuf, arachide, fruits à coque, poisson, ...) le sésame.
Pour les tests épicutanés on fera la batterie standard européenne à laquelle on associera les tests épicutanés alimentaires et les aéroallergènes.
Les sensibilisations les plus fréquemment retrouvées sont les acariens, le nickel, la lanoline, les parfums, l’émollient utilisé. Pour les tests épicutanés alimentaires on utilisera des cupules de 12 mm et l’aliment natif.
La valeur des IgE spécifiques est importante car elle doit nous guider dans la prise en charge ultérieure. La concentration des IgE prédictive d’une réactivité est toute fois différente selon les équipes et doit donc être adaptée.
La référence reste le test de provocation orale, mais qui reste un test dangereux à ne faire que dans un service spécialisé.
– Les tests allergologiques : pourquoi ?
Le bilan allergologique est essentiel pour la prise en charge thérapeutique.
Il permet d’identifier les enfants ayant une forme favorable. Il identifie les formes persistantes et à risque de développer d’autres manifestations atopiques. Les tests allergologiques précisent les enfants pouvant bénéficier d’une prévention secondaire.
– En conclusion : On retrouve des facteurs allergiques dans 30 à 40 % des EA. Il faut explorer le versant immédiat et retardé. La prise en charge est locale et globale. Le suivi ultérieur est indispensable.
Désensibilisation sublinguale : place et limite
Pr Alain Didier, Toulouse
La désensibilisation sublinguale a surtout été étudiée depuis 1999. On assiste à une envolée des publications depuis 2003.
– Efficacité de la désensibilisation sublinguale
La désensibilisation sublinguale rentre dans les recommandations ARIA 2001 avec un niveau A pour la rhinite saisonnière chez l’enfant. Pour la rhinite perannuelle il n’y avait pas assez de publication lors de la mise en place des recommandations.
Dans la méta-analyse de la Cochrane review 2003 on retrouve 33 études publiées dont 22 retenues, 6 pour les acariens, 5 pour les graminées, 5 pour la pariétaire ...Malheureusement cette méta-analyse comprend 152 enfants ce qui n’est pas suffisant. Cette étude montre une efficacité avec un p = 0,02 pour l’ensemble, essentiellement pour les allergies saisonnières.
– Comparaison voie sublinguale et sous-cutanée
Deux études, l’étude de Mungun en 1999 avec les acariens et l’étude de Kinchi en 2004 sur le pollen voir plus – Définition de bouleau ont montré l’équivalence entre la désensibilisation sublinguale et sous-cutanée et leur supériorité par rapport au placebo.
Les effets secondaires étaient plus fréquents et plus graves avec la désensibilisation par voie injectable.
Avec la voie sublinguale, les effets systémiques sont très rares. Les effets locaux sont assez fréquents à type de brûlures, de picotements parfois de troubles digestifs qui le plus souvent n’amènent pas à interrompre le traitement. On peut également avoir une urticaire limitée au menton.
– Modification de l’histoire naturelle
On sait que la désensibilisation par voie sous-cutanée peut modifier la carrière allergique (Etude de Moller JACI 2002). Dans son étude, Di Rienzo (Clin Exp allergy 2003 ; 33 : 206-10) montre sur 60 enfants désensibilisés une différence significative persistante sur 10 ans.
– Mode d’action
Pajno montre que la désensibilisation par voie sub-linguale diminue l’hyperréactivité bronchique pendant la saison pollinique dès la deuxième année (Allergy 2004 ; 59 : 883-887).
– En conclusion
La désensibilisation a montré son efficacité persistante, mais reste à définir la dose, la durée, le mécanisme... Les études en population pédiatrique sont encore peu nombreuses. Il est donc important d’avoir d’autres études.
Éviction des acariens en pratique
Dr Agnès Juchet, Toulouse
Il faut une éviction globale et supérieure à 6 mois des acariens pour avoir un retentissement clinique. Cette éviction est certainement plus efficace chez l’enfant. Mais que faut-il faire exactement ?
– En premier il faut lutter contre l’humidité.
Les conditions idéales de développement des acariens sont de 55 à 75 % d’humidité avec une température de 22 à 28 °.
À partir de 1 500 mètres d’altitude, on ne retrouve plus d’acariens.
Il faut donc aérer avant tout. Pour vérifier les bouches d’aération, on peut simplement mettre un papier toilette devant et vérifier qu’il est bien aspiré. Il faut vérifier que les réglettes au-dessus des fenêtres sont bien débouchées.
– Le contrôle de la literie est important.
On conseillera un sommier à lattes avec un matelas en mousse dense et une housse anti-acarien. Celle-ci sera en poly-uréthane microporé et doit entourer complètement le matelas.
Les housses anti-acariens des grandes surfaces sont souvent simplement en coton imbibé d’un acaricide qui va disparaître au bout de 3 à 4 lavages. Elles sont donc à déconseiller.
La housse doit être lavée tous les 3 mois à 60 °C. Elle est garantie 10 ans, mais ne doit pas passer au sèche-linge.
Les draps doivent être lavés toutes les semaines. Il faut utiliser des oreillers et des couettes synthétiques lavables ou des couvertures polaires. L’idéal est de les laver à 60 ° C sinon on peut les laver à 30 °C avec un produit acaricide. Il faut éviter le lavage à sec.
Les jouets doivent être rangés dans un bac. Il faut éviter les fauteuils capitonnés les doubles rideaux et préférer les voilages. Il faut mettre au congélateur puis laver les peluches (3 maximum). Le mieux est de ne pas avoir de moquette mais sinon, on peut faire un Acarex-test (20 euros les 10 tests). S’il est à ++ ou +++ il faut enlever la moquette. S’il est à + on peut traiter. Attention aussi aux mousses sous le parquet stratifié.
– Le ménage doit être fait avec un ballet avec chiffon microfibre, L’aspirateur est plus néfaste car il relargue les acariens sauf ceux qui sont à filtre HEPA qui peuvent maintenant être achetés en supermarché à des prix quasi-identiques.
– Les acaricides sont tous toxiques pour les voies respiratoires. Il faut les laisser agir 1 à 2 heures, aérer puis aspirer soigneusement. Le mieux est d’attendre 24 heures avant que l’enfant ne revienne dans sa chambre.
Nouveautés thérapeutiques en allergie alimentaire : Anti-IgE, désensibilisation, ...
Dr Fabienne Rancé, Toulouse
Fabienne Rancé à préférer élargir le sujet au traitement de l’allergie alimentaire.
– Les soins d’urgence reposent sur les anti-histastaminiques H1 en cas d’urticaire aiguë, d’angio-œdème, de rhinite ou de conjonctivite sans signes d’asphyxie, les broncho-dilatateurs en cas de crise d’asthme, le stylo auto-injectable en cas d’œdème laryngé avec signes d’asphyxie ou de choc anaphylactique.
Le stylo auto-injectable Anapen n’étant disponible qu’en deux dosages 0,15 mg et 0,30 mg, on se retrouve fréquemment en sous-dosage ou en surdosage.
– Le traitement des allergies alimentaires repose sur le traitement des symptômes, le traitement préventif (régime d’éviction, éducation mais pas de traitement médicamenteux) et le traitement étiologique.
La directive de la CE 2003 applicable en Novembre 2005 doit permettre l’authentification de 12 allergènes sur tous les produits alimentaires.
À l’école, le PAI (circulaire de 2003) permet l’intégration de l’enfant allergique à l’école et lors de la restauration scolaire.
Les nouveautés 2004 comprennent l’adaptation des plats en fonction des allergies alimentaires. Des menus spéciaux (paniers-repas, repas sécurisé) doivent être donnés en cas de réaction lors d’inhalation, de polyallergies ou de réactions à des quantités minimes. Les enfants au comportement non adapté ou ayant des réactions graves ne peuvent bénéficier de la restauration scolaire. Sinon il faut adapter les plats en particulier après consultation des menus par le personnel de restauration scolaire et par les parents.
– Le traitement vaccinal n’a pas montré son efficacité actuellement. Oppenheimer avait tenté un traitement vaccinal en 1992 qui s’était soldé par un décès. En 1997 la même équipe publie une étude sur 12 patients (6 placebos) avec un effet maintenu, mais les effets secondaires systémiques sont constants nécessitant souvent le recours à l’adrénaline (JACI 1997 ; 99 : 744-51).
– Parmi les nouveaux traitements, les anti-IgE (TNX-90) à la dose de 450 mg permettent une diminution de la dose déclenchante et une diminution des autres allergies alimentaires. Mais le traitement doit être maintenu à vie.
Les probiotiques pourraient être intéressant. Une étude Finlandaise montre une diminution des eczémas atopiques (46 versus 23, p = 0,008) en cas d’atopie familiale et de traitement par Lactobacillus GG avant et après l’accouchement. Par contre il n’y a pas de différence en terme de sensibilisation. Quand on compare plusieurs mixtures associant en particulier du Lactobacillus GG (LGG) et du rhamnosus seul le LGG modifie le profil allergénique.
Toutes ces nouvelles approches thérapeutiques nécessitent de contrôler la toxicité, l’éventuel développement de maladies auto-immunes, les effets à long terme ...
On ne peut conclure sans parler des allergènes recombinants qui vont certainement marquer un progrès dans notre prise en charge.
Recevez les actualités chaque mois